Тип урока: Интегрированный урок совершенствования знаний, умений и навыков.
Вид урока: Урок-семинар с элементами практической работы, межпредметных связей с географией и биологией.
Цель урока: Обобщить и повторить с учащимися пройденный материал о солях.
Задачи:
- Образовательные: проверить качество и порочность знаний учащихся по теме "Соли".
- Развивающие: развивать логическое мышление путём сравнения, обобщения, синтеза, развития мобильности, самостоятельности, умение рефлектировать, развивать правильную речь, навыки самоконтроля .
- Воспитательные: формировать умение работать с книгой; показать учащимся межпредметную связь и практическую направленность, изучаемого материала.
Средства обучения:
1. Реактивы и оборудование: растворы кислоты (HCl), щелочи (NaOH) и соли (NaCl), универсальный индикатор, стеклянная палочка, пробирки, штатив, лепестки фиалки.
2. Мультимедийный проектор, компьютер, презентация PowerPoint.
3. Ветка кораллов, карта.
ХОД УРОКА (45 МИНУТ)
1. ОРГАНИЗАЦИОННЫЙ МОМЕНТ УРОКА (3 МИН.)
Учитель химии: "Слеп физик без математики, сухорук без химии" - говорил М.В.Ломоносов. Спустя много лет, другой русский ученый В.И.Вернадский продолжил эту мысль словами: "...рост научного знания быстро стирает грани между отдельными науками".
Сегодня на уроке мы найдем одну из общих точек соприкосновения между тремя науками: химия, биология, география. Такие, разные на первый взгляд, науки имеют много общего. Более того, академиком Вернадским создана наука о связи живых организмов с неживой природой, называемая биогеохимия. Эта взаимосвязь и отражена в эмблеме нашего урока.
Темой нашего урока будут соли. Сегодня на уроке мы повторим составление формул солей, их названия, практическое применение некоторых из них, проведем небольшую практическую работу по распознаванию солей. А также покажем значение солей в неживой и живой природе.
2. ХИМИЧЕСКАЯ РАЗМИНКА (12 МИН.)
I. Слайд № 1
NaCl ,CaCO3 , AgNO3 ,CuSO4 ,MgSO4 , Na 2CO3 ,BaCl2 ,BaSO4, CaCl2,Ca3(PO4)2 , NaI.
( называют поочередно)
а) Прочитать формулы солей.
б) Назвать соли.
В) Найти нерастворимые соли (с использованием таблицы растворимости).
II. Составить формулы солей и дать им название
(Два ученика работают у доски, остальные учащиеся - на своих местах.)
а) Zn xCly, Cax(CO3 )y;
б) KxSy, Nax(SO4)y.
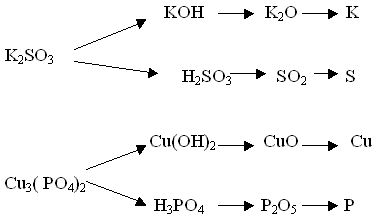
III. Работа с учебником (упр.3, стр. 77). Выписать из предложенных веществ формулы солей. Назвать их и определить соответствующие им кислоты, основания, оксиды и простые вещества. (работа у доски 2 сильных учащихся)
3. Соли в окружающем мире (сведения о солях из дополнительной литературы, использование ресурсов Интернета)
Учитель химии: Давайте поговорим о практическом значении некоторых солей, которые представлены. Что вам известно о них?
NaCl (Слайд № 2)
1 ученик:.NaCl - единственное минеральное сырье, которое человек использует в пищу в чистом виде. Когда живые организмы вышли на сушу, они сменили богатую хлоридом натрия среду. в которой жили, на бедную этой солью среду - на сушу, Поэтому живому организму необходимо искать NaCl в крови другого животного, как это делают хищники, Или добывать в чистом виде, как это делают травоядные и всеядные, а также человек.
Учитель биологии: С точки зрения биологии, хлорид натрия активно участвует в минеральном обмене организма животного и человека. Он содержится в крови, пищеварительном соке. В организме человека соли составляют 5,5% массы тела, в том числе хлорида натрия около 300 г. Среднесуточная норма потребления хлорида натрия взрослого человека - 15 г. Зв год человек съедает 5-7 кг соли.
2 ученик: NaCl стимулирует обмен веществ, рост волос, придает бодрость и силу .Недостаток его в организме вызывает головокружение, обмороки, нарушение работы сердца, снижение аппетита, уменьшение воды в крови и органах, сокращение выделения пищеварительного сока. При употребление 10-кратного избытка соли она превращается в смертельный яд.
Учитель географии: На уроках географии мы рассматриваем NaCl как минерал. А что такое минерал?
3 ученик: Минерал - это природное соединение химических элементов, образовавшиеся естественным путем без вмешательства человека.
NaCl - минерал галит (от гречес. "галос" - соль). Полупрозрачен, со стеклянным блеском, бесцветен, но примеси часто окрашивают его в серый, красный, коричневый цвета. Красивая голубоватая и фиолетовая окраска некоторых галитов связана с воздействием на них радиоактивных лучей в природных залежах. ( Показ минерала)
Учитель географии: Соль известна людям давно. Вот несколько известных фактов.
4 ученик: Некоторые народы Центральной Азии в своё время платили за соль цену примерно равную цене золота.
5 ученик: В Китае за 2 тысячи лет до нашей эры впервые начали добывать соль из морской воды. А в средние века в Китае были крестьянские волнения, вызванные непомерными солевыми поборами, которые продолжались 9 лет.
6 ученик: В Эфиопии вплоть до XIX века находились в обращении соляные деньги - бруски NaCl . А в Древнем Риме воины Цезаря часть зарплаты получали солью.
Учитель географии: Но поскольку мы с вами изучаем географию нашей Родины, то хотелось бы поговорить о залежах и методах добычи соли у нас. Есть два вида хранилищ соли - древние и современные. Древние, или ископаемые соляные месторождения,
состоят из залежей, которые образовались много миллионов лет назад. Нередко они занимают площади в десятки и сотни квадратных километров. И при этом обладают мощностью до 1 км и более. В Прикаспии такие соляные купола имеют глубину 9-10 км Место выхода куполов прикрыто озерами. Современные месторождения - соляные озера и бассейны, в которых осаждение солей началось сравнительно недавно и еще продолжается. У нас соляной пояс - от низовья Дуная до Забайкалья. К числу современных соляных бассейнов относятся заливы Черного, Азовского и Каспийского морей, озера Эльтон, Баскунчак (Пермская, Оренбургская, Волгоградская, области дают основную часть всей добычи соли России) (показ на карте).
А чем знаменито озеро Эльтон?
7 ученик: Когда - то через Покровскую слободу пролегала Великая соляная дорога - нынче проспект Строителей в г. Саратове; а начиналась она на Ю.-В. В трех верстах от озера Эльтон. (показ на карте)
Сегодня его берега малолюдны, промыслы перенесены на Баскунчак. А вот два с половиной века тому назад у кромки Эльтонских соляных вод располагался целый городок, население доходило до 3-4 тыс. человек. Ломщики с самого раннего утра уплывали к месту, где замечены были самые хорошие слои. Ломали, откалывали от пластов глыбы и сдавали на склад. За 9 месяцев (с апреля по декабрь) от Покровска на озеро и обратно упрягали верблюдов, волов, лошадей, успевая сделать по 5 рейсов. Длина дороги была 307 км., ширина - 40 м. За 134 года работы было добыто 513 млн. пудов соли (3 тыс. железнодорожных составов).
Учитель географии: Так что образованию нашей малой родины мы обязаны полковнику Чемодурову и NaCl. А к 250- летию города был утвержден герб, на котором вол везет телегу с солью.
CaCO3 (Слайд № 3)
8 ученик: Это белое кристаллическое вещество, нерастворимое в воде. Это и школьный мел, мрамор, известняк. яичная скорлупа, жемчуг.
Учитель биологии: Карбонат кальция входит в состав наружного скелета морских звезд, кораллов, раковин, двустворчатых и брюхоногих моллюсков, панцирей морских ежей и скелетов микроорганизмов, которые, отмирая, опускаются на дно и скапливаются там, постепенно превращаясь в залежи известняка и мрамора.
9 ученик: Земледельцы давно заметили, что на почве, посыпанной известняком, растения чувствуют себя лучше. Особенно это важно для молодых растений. Без кальциевых солей их корни делаются вялыми, быстро загнивают. Потому - то молодое растение жадно впитывает в себя эти соли, ему надо окрепнуть. А к старости в стволе и корнях накапливается много кальциевых солей. Они и придают деревьям прочность.
Учитель географии: Карбонат кальция это сталактиты и сталогмиты. Когда подземные воды растворяют соли (гипс, известняки, доломиты) образуются карстовые котловины, воронки, пещеры. (От названия известнякового плато Карст на северо-востоке от горы Триест на побережье Адриатического моря, где впервые были изучены). На дне и потолке пещер можно найти твердые окаменевшие формы. Вода просачивается через трещины пород, которые она растворяет. Так образуется сосулька, свешивающаяся с потолка - сталактит. А навстречу ей снизу растет другая, более широкая и плоская - сталагмит. Срастаясь, они образуют целый ансамбль колонн (показ фотографий). Узорчатые, витые, словно сплетенные из кораллов, колонны целыми букетами поднимаются кверху по стенам и углам. Со сводов свешиваются каменные люстры. При свете свечей или фонарей все эти украшения переливаются. Причудливые тени сталактитов и сталагмитов, придают подземелью таинственный вид.
Иногда карбонат кальция покрывает стены пещеры в виде муки - "горная мука". Если частички его взвешены в воде, получается "лунное" или "горное молоко".
В пещерах встречаются причудливые скопления CaCO3 , похожие на виноградные гроздья - "каменный виноград".
Учитель географии: (показ веточки кораллов) А где применяются кораллы?
10 ученик: Кораллы широко используются в ювелирном деле. Особенно ценится благородный коралл, окрашенный в розовый или красные цвета. На востоке высоко ценится амулеты и четки из черного коралла. В виде порошка раньше применяли при болезни кишечника и желудка. В последние годы из белых кораллов японские стоматологи стали изготавливать искусственные зубы. Они не окисляются и не разрушают ткани ротовой полости. Иногда белые кораллы используют в качестве заменителя кости. Коралл не отчуждается организмом и приживается лучше, чем протезы из пластмассы и искусственного материала.
Ca3 (PO4)2 (Слайд № 4)
11 ученик: Это твердое белое кристаллическое вещество, нерастворимое в воде. Нам известно, что это главный конструкционный материал для построения внутреннего скелета позвоночных, костей, зубов.
Учитель биологии: Фосфат кальция содержится в мышцах, нервах, особенно необходим для построения скелета ребенка. Нехватка этой соли в организме человека и животного приводит к заболеванию рахитом. Источниками фосфата кальция являются такие продукты как сыр, говядина, печень, рыба, белый хлеб, яйца, молоко, йогурт.
Na2CO3 (Слайд № 5)
12 ученик: Карбонат натрия - кальцинированная сода. Белое твердое кристаллическое вещество, хорошо растворимое в воде, бытовое название - стиральная сода. В природе встречается в виде минералов: натрон, а также в составе рапы соляных озер. Используется в производстве стекла, моющих средств, для смягчения воды.AgNO3 (Слайд № 6)
13 ученик: Нитрат серебра - белое твердое кристаллическое вещество, медицинское название - ляпис. Он обладает прижигающим и вяжущим действием, т.к. взаимодействует с белками тканей, способствует образованию белковых солей - альбуминатов. Свойственно ему и бактерицидное действие. Поэтому ляпис широко применяют в медицинской практике для выведения бородавок. А также используют при изготовлении зеркал и получении токопроводящего слоя.
CuSO4 (Слайд № 7)
14 ученик: Твердое кристаллическое вещество голубого цвета, хорошо растворимое в воде, историческое название медный купорос. Его добавляют в побелку при ремонте. Применяют на огороде против болезней и вредителей растений. Медный купорос, как и другие, соли меди ядовит, особенно для низших организмов. При добавке его даже в незначительном количестве в аквариум с водорослями они погибают.
Учитель биологии: Соли меди необходимы в организме для синтеза пигментов, окрашивающих кожу, глаза, волосы, кроме того они регулируют работу желез внутренней секреции, белковый обмен. Соли меди поступают в организм человека с продуктами: черный хлеб, картофель, шоколад, соя, кокосовый орех, кофе, печень. Суточное потребление меди 2-3 мг.
MgSO4( Слайд № 8)
15 ученик: Сульфат магния - горькая английская соль. Белое твердое кристаллическое вещество, хорошо растворимое в воде, в большом количестве содержится в морской воде, придавая ей горький вкус.
Учитель биологии: Магний называют антистрессовым металлом. Соли магния предупреждают атеросклероз, сердечно-сосудистые болезни, предохраняют клетки от губительного воздействия стресса, способствуют эластичности мышц и росту тканей.
В наш организм соли магния поступают с продуктами: фасоль, горох, орехи, крупы, мед, зелень, хлеб, морепродукты. Суточное потребление магния 0.3-0.7г.
NaI (Слайд № 9)
16 ученик: Иодид натрия - белое твердое кристаллическое вещество, хорошо растворимое в воде. Добавляют в поваренную соль для предупреждения заболеваний щитовидной железы.
Учитель биологии: Йод - элемент, без которого человек не может жить. Недостаток в организме йода приводит к такому тяжелейшему заболеванию, как опухоль щитовидной железы - зоб. Самыми большими любителями йода оказались скромные морские водоросли ламинарии. Соли йода поступают в организм человека с морской капустой, йодированной солью, морской рыбой, шампиньонами.
Прием натуральных продуктов не вызывает побочных эффектов, даже при избыточном содержании в них йода. В норме в организме человека содержится 15-25 мг йода, причем половина в щитовидной железе.
BaSO4 (Слайд № 10)
17 ученик: Сульфат бария - белое кристаллическое вещество , нерастворимое в воде. Благодаря нерастворимости и способности задерживать рентгеновские лучи применяют в рентгенодиагностике для диагностики заболеваний желудочно-кишечного тракта. Заполняя пищевод, а затем желудок и кишечник, баритова каша (смесь сульфата бария с водой) ,непрозрачная для рентгеновских лучей,"проявляет" контуры органов пищеварения, что позволяет ставить диагноз их заболеваний.
CaCl2 (Слайд № 11)
18 ученик: Хлорид кальция белое твердое кристаллическое вещество, растворимое в воде. Эта соль способствует свертыванию крови. Применяется в медицине. Оказывает противовоспалительное, противоаллергическое и успокаивающее действие, уменьшает проницаемость сосудов.
Учитель химии: Соли широко применяются в быту (сода, поваренная соль, ацетат железа, бура, квасцы), в сельском хозяйстве в виде удобрений (селитра, поташ), в строительстве (мел, мрамор, гипс, известняк), в химической промышленности, в медицине (фторо - йодистая соль, диетическая соль, поваренная соль), а также играют огромную роль в построении и работе всех органов тела.
4. Практическая работа
Техника безопасности (учитель химии):
Вы будете работать с кислотами, щелочами. Следует помнить, что вещества нельзя подносить близко к лицу, пробовать на вкус, проливать на кожу и одежду.
Задание:
Реактивы на столах: растворы кислоты (HCl), щелочи (NaOH) и соли (NaCl). С помощью универсального индикатора определить, в какой пробирке находится соль.
Опустите индикаторную бумагу в пробирки. Что наблюдаете? Сделайте вывод.
Учитель химии: (Слайд № 12)
А знаете ли вы, что кроме химических индикаторов существуют природные? Многие ягоды (вишня, черноплодная рябина, смородина), цветы (ириса, анютины глазки, тюльпаны, цветы герани, пиона, фиалки, василька) имеют в кислой среде розовую окраску, а в щелочной становятся синими. Это природные индикаторы.
(Показ опыта учителя с фиалкой, ее лист становится розовой при опускании в раствор с кислотой)
5. Самостоятельная работа
Учитель химии: Сейчас мы проведем небольшую самостоятельную работу. Я прочту небольшой текст. А ваша задача выписать формулы названных мною солей и географических названий.
Многие минералы, входящие в состав литосферы, являются солями. Только геологи дали этим минералам свои геологические названия.
Минерал чилийская селитра представляет собой нитрат натрия. Свое название он получил по названию страны, имеющей большие запасы чилийской селитры
Кольский полуостров богат фосфорными рудами, в частности, апатитом. Это не что иное, как фосфат кальция. Вблизи огромного месторождения построен город, который так и называется Апатиты.
Когда-то территория нашей Саратовской области была дном мирового океана. Известковые панцири морских моллюсков, раковин, рачков представляют собой карбонат кальция. Отмирая, морские обитатели опускались на дно, их скелетные ткани образовывали огромные пласты минерала- известняка. Он широко используется в промышленности и строительстве.
Учитель химии: После выполнения поменяйтесь работами с соседом, сидящим справа от вас. Сверьте ответы вашего соседа с ответами на доске выставьте оценки.
(Слайд № 13)
6. Практические советы
Учитель химии:
Чтоб знания о солях вы могли использовать в повседневной жизни, мы хотим дать вам несколько полезных советов.
1. Чтобы белье лучше отстиралось. А цветное при стирке неполиняло, его необходимо предварительно замочить в соленой воде.
Учитель биологии:
2. Чтоб защитить мясо, рыбу, овощи от порчи, необходимо обильно посыпать их солью. Чтоб махровые полотенца и халаты были мягкими, а у вас нет "Линора", вам необходимо стирать их в слегка соленой воде.
Учитель географии
3. Чтобы водопроводные трубы на кухне и ванной не плесневели, нужно добавить в краску минерал буру (натриевая соль борной кислоты). Если ремонта в ближайшее время не предвидится, протрите трубы раствором медного купороса. Это ненадолго защитит их от появления плесени.
7. Выводы, обобщение, заключение.
Рефлексия.
- Беседа по вопросам:
- Что нового вы узнали сегодня на уроке?
- Что запомнилось?
- Что понравилось, а что не удалось, на ваш взгляд?
Поведение итогов.
- Выводы по уроку.
- Оценки за урок химии, биологии, географии.
- Знакомство с дополнительной литературой по изучаемой теме.
Список литературы.
- Казаков Б.И. Страницы летописи Саратова. Саратов:Приволж. кн. изд-во, 1987 с.41-49
- Егоров А.С., Иванченко Н.М., Шацкая К П. Химия внутри нас. Ростов-на-Дону: Феникс 2004
- Скальный А.В. Химические элементы в физиологии и экологии человека. "ОНИКС 21 век" 2004
- Я познаю мир: Детская энциклопедия: химия АСТ-ЛТД 1997