Химическое превращение, химическая
реакция - есть главный предмет химии.
Семенов Н.Н.
Тема урока: химические реакции в органической химии
Главная дидактическая цель: формирование умений самостоятельно приобретать знания, используя различные источники информации.
Главная развивающая цель: развитие творческого мышления, внимания, активности учащихся.
Главная воспитательная цель: формирование опыта делового общения, творческой деятельности.
Задачи урока:
- Формирование умений выделять и планировать этапы учебного исследования;
- Учить самостоятельности прогнозирования результатов;
- Развивать умения и навыки коллективного творчества.
Форма урока: мастерская построение знаний.
Методы: частично проблемно-поисковый, словесный, практический, письменного контроля.
Приемы: беседа, прогнозирование, детальное изучение.
Оснащение урока: учебник, ряд электроотрицательности, набор шаростержневых моделей, интерактивная доска, магнитная доска.
Прогнозируемый результат:
Учащиеся должны:
- Уметь работать со шаростержневыми моделями;
- Уметь классифицировать химические реакции по основным признакам;
- Уметь видеть общее и различное при классификации реакций в органической и неорганической химии;
- Научиться сравнивать, анализировать, обобщать.
Ход урока
I. Повторение: 7-10 минут;
II. Новый материал: 50 минут;
III. Закрепление материала: 15-20 минут;
IV. Итог, домашнее задание:10 минут.
I. Повторение:
Классификация химических реакций в неорганической химии:
1. По числу и составу исходных веществ и продуктов реакции:
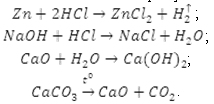
2. По тепловому эффекту, присутствие катализатора, обратимости процесса, о-в реакции:
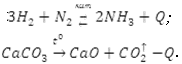 .
.
2. Новый материал
Сохраняются ли на ваш взгляд все эти признаки химических реакций для органических веществ?
Определите тип реакций в приведенных уравнениях (5 минут):
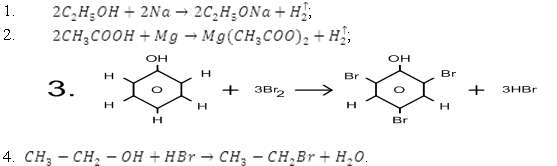
Четвертая реакция не относятся к реакции обмена - это реакция замещения
Понятие «замещения» в органической химии – шире. Если в молекуле исходного вещества какой-либо атом или функциональная группа заменяются на другой атом или группу, это тоже реакция замещения.
Многие процессы в органической химии можно формально отнести к одному из четырех типов:
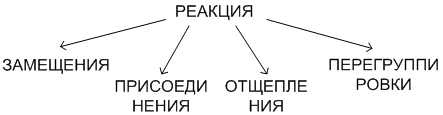
Прежде чем мы их рассмотрим, давайте вспомним:
- Какие углеводороды вы знаете;
- Почему углеводороды называются предельными (насыщенными) и непредельными;
- Какие виды (
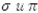 ) связи присутствуют в молекулах углеводородов.
) связи присутствуют в молекулах углеводородов.
Вспомним характеристики связей ![]() (на столе раздаточный материал) (5 минут)
(на столе раздаточный материал) (5 минут)
| Сравнительная характеристика связей | |||
Характеристика |
Вид связи |
Варианты ответов |
|
|
|
||
Образование связи |
|||
Вид перекрывания Орбитали, участвующие в образовании связи |
|
|
Осевое или боковое |
|
|
|
|
Особенности связи |
|||
Прочность |
|
|
Высокая или невысокая Высокая или низкая |
Какие вещества (с наличием какого вида связи) могут вступать в реакцию замещения и присоединения?
Вывод. В реакции замещения могут вступать вещества в том случае, если между атомами, вступающими в реакцию замещения, присутствуют ![]() -связи, а в реакции присоединения вещества с наличием
-связи, а в реакции присоединения вещества с наличием ![]() - связи
- связи
Перейдем к реакциям присоединения и отщепления, но сначала найдем определение понятий: субстрат, реагент, элиминирование (запись понятий в словари дома).
Эти два типа реакций изучим в сопоставлении (у вас на столах шаростержневые модели, алгоритмы (Приложение 1), задание (Приложение 2).
Прочитаем первое правило алгоритма.
Реакция – это разрыв одних связей и образование других.
Вспомним, как может происходить разрыв связи:
1) Гомолитический;
2) Гетеролитический.
Что такое радикал?
1. Нуклеофилы
любящий протон, положительный заряд;
2. Электрофилы
любящий электрон, отрицательный заряд.
Чтобы немного прояснить полученную информацию, выполним задание (5 минут). Среди указанных частиц определите радикальные, электрофильные и нуклеофильные реагенты:
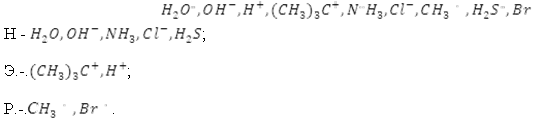
А теперь, имея алгоритм и шаростержневые модели атомов, попробуем получить продукты и назвать их (используйте правила на стр.86 и 88) (20 минут).
(На магнитной доске обозначение цветов: белый – Н, черный –С, серый –О, желтый – CI, калий - K , серый - Zn , зеленый - Na).
Сравним полученные результаты с записью на доске.
(Запись на доске учителем продуктов реакции и сравнение с полученной шаростержневой моделью у учащихся).
При рассмотрении реакции гидрогалогенирования могут получиться разные продукты. Почему?
Рассмотрим еще один пример реакции присоединения. Возьмем две молекулы пропилена.
Какой тип реакции характерен для веществ, имеющих ![]() - связь-присоединения, по месту разрыва
- связь-присоединения, по месту разрыва ![]() - связи.
- связи.
Как вы думаете, может ли присоединяться друг к другу больше чем две молекулы? (Может).
Это реакция полимеризации. (стр.45).
Одним из примеров полимеризации – сополимеризация (в образовании полимера участвуют различные мономеры).
Последний тип реакции, в которых исходные органические соединения сохраняют свой молекулярный состав, но изменяют химическое строение.
Как называются такие вещества? (изомеры), а реакция называется - изомеризацией.
Наиболее простой и наглядный пример реакции изомеризации – превращение бутана нормального строения в изобутан (при нагревании в присутствии катализатора):
![]() .
.
Превращение алканов с неразветвленной цепью в углеводороды с разветвленным углеродным скелетом – очень важный промышленный процесс, называемый риформингом.
Кроме приведенных базовых типов реакций мы с вами встретимся с другими терминами, отражающими специфику процессов: окисления, восстановления, конденсации, пиролиз, крекинг и.т.д.
III. Закрепление.
Выполнение проверочной работы. (Приложение 3).
IV. Домашнее задание.
1. Закончить уравнения реакций:
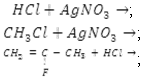
2. Вспомнить классификацию оксидов и гидроксидов.