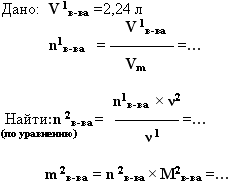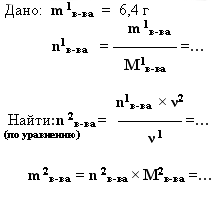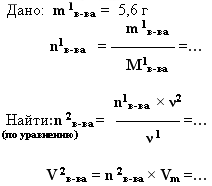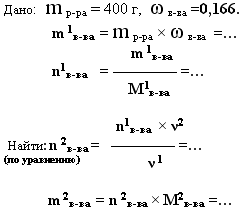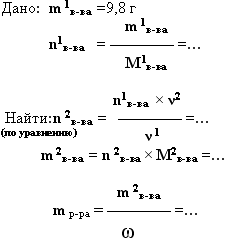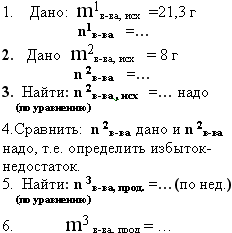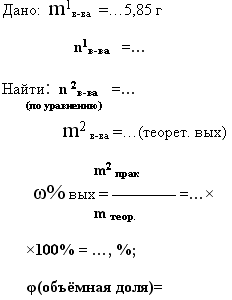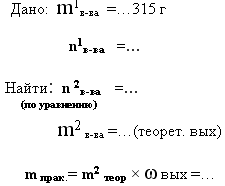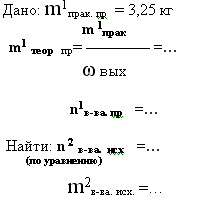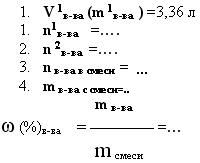Расчеты по формулам.
-
Какое из следующих соединений
содержит больше железа: FeO,
Fe2O3,
Fe3O4.
- Сколько железа содержится в 5 моль
оксида железа (III).
- Выведите формулу соединения,
состоящего 88,85% из меди и 11,2% -
кислорода.
- Массовое соотношение калия,
углерода и кислорода в веществе – 39:
6: 24. Какова формула вещества.
- Сколько граммов воды выделится при
прокаливании 644 г глауберовой соли Na2SO4*10
H2O.
- Сколько граммов кальция содержится
в 250 г карбоната кальция?
|
-
*Сколько граммов кальция
содержится в 300,0 г известняка,
содержащего 90% карбоната кальция?
- *Минерал содержит 96% CuS.
Какую массу этого минерала необходимо
переработать, чтобы получить 100 г меди.
- *Из 1 т глинозёма, содержащего 95%
оксида алюминия, получили 0,436 т
алюминия. Каков процент выхода?
- *Сколько потребуется магнитного
железняка, содержащего 90% Fe3O4
для получения 100 т железа, если потери
в производстве составляют 3%.
|
Расчёты по уравнениям:
1. дано: n(моль) –
найти: n(моль).
|

|
-
Сколько моль оксида меди получится
при полном окислении 3 моль меди?
- Какое количества вещества
гидроксида железа (III)
разложилось, если получили 0,5 моль
оксида железа(III)?
- Сколько моль кислорода потребуется
для полного окисления 2,5 моль
алюминия.
- При электролизе хлорида меди
получили 3 моль меди. Сколько моль
хлора при этом выделилось.
|
2. дано: m (г, кг, т)
– найти: m (г, кг, т).
|
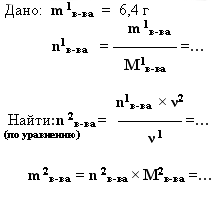
|
-
Вычислите массу оксида меди
полученного при окислении 6,4 г меди.
- Сколько оксида серебра необходимо
прокалить, чтобы получить10,8 г
серебра.
- Какая масса гидроксида железа (III)
выпадет в осадок, если на раствор,
содержащий 16,25 г хлорида железа(III)
подействовать раствором гидроксида
натрия.
- Вычислите, достаточно ли 6,4 г
кислорода для полного обжига 9,6 г
сульфида цинка.
|
3. дано: m (г, кг, т)
– найти:V (мл, л, м3).
|
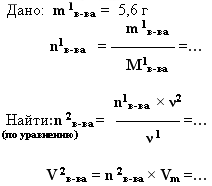
|
-
При обжиге известняка было
получено 5,6 г оксида кальция. Какой
объём углекислого газа(н.у.) при этом
образовался.
- Какой объём хлора потребуется для
полного сжигания 5,6 г железа?
- 10,6 г соды растворили в соляной
кислоте. Какой объём углекислого
газа при этом выделился?
- Сколько кислорода потребуется для
сжигания 3 г лития?
|
4. дано: V (мл, л, м3).–
найти: m (г, кг, т)
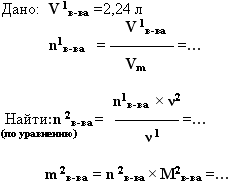 |
-
Цинк растворили в соляной кислоте,
и объём выделившегося газа составил
2,24 л (н.у.). Какая масса цинка была
растворена?
- На восстановление меди их оксида
меди(II) было
израсходовано 5,6 л водорода. Сколько
граммов меди получили?
- Достаточно ли 2,8 л оксида углерода (II)
для полного восстановления железа из
23,2 г Fe3O4.
Какой объём углекислого газа при этом
образуется?
|
5. дано: m р-ра(смеси)
и ω (%)в-ва(примеси)
- найти: mв-ва
или V в-ва
|
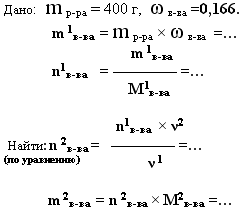
|
-
В 400 г 16,6 %-ного раствора азотной
кислоты, растворили гидроксид меди(II).
Какая масса соли получилась?
- Какой объём углекислого газа
выделится при обжиге 120 г известняка,
содержащего 5 % примесей?
- *Какая масса гидроксида алюминия
выпадет в осадок при взаимодействии
с раствором щелочи 150 г раствора
сульфата алюминия, массовая доля
соли в котором 22,8%. Какая масса
гидроксида натрия должна быть в
растворе щелочи.
|
6. дано: mв-ва
(или V в-ва),
ω (%)в-ва - найти: m
р-ра
|
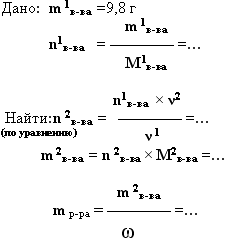
|
-
Какую массу 40% раствора гидроксида
натрия необходимо взять, чтобы
нейтрализовать 9,8 г серной кислоты.
- Какую массу 6%-ного раствора
сульфата железа(III)
необходимо взять для реакции с
гидроксидом калия, чтобы получить 10,7 г
гидроксида железа(III).
- Какую массу известняка содержащего
5% некарбонатных примесей, необходимо
разложить, чтобы получить 44,8 л оксида
углерода (IV).
- *Оксид кальция содержит 5 %
карбонатных примесей. Какой объём
углекислого газа выделится, если 20 г
его растворить в соляной кислоте?
|
7. дано: m1в-ва
и m2в-ва
- исходные вещества (какое-то их них
находится в избытке)
найти: m3
в-ва продукт реакции.
|
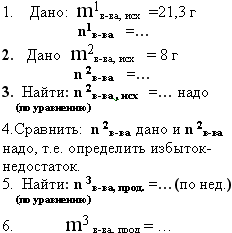
|
-
К раствору, содержащему 21,3 грамм
нитрата алюминия, прилили раствор,
содержащий 8 грамм гидроксида натрия,
определите массу полученного осадка.
- В раствор, содержащий 40 грамм
сульфата меди (2) добавили 12 грамм
железных опилок, рассчитайте массу
полученной меди.
- *Какой объем газа выделится, если к
раствору, содержащему 53 грамма
карбоната натрия, прилили 400 грамм 20 %
азотной кислоты.
- *К 100 грамм 6% раствора гидроксида
натрия прилили 200г 10% раствора
сульфата железа (3), вычислите массу
образовавшегося осадка.
|
8. дано: m1в-ва
исход. и m2в-ва
- продукта реакции- практический выход -
найти: m2
в-ва продукта реакции- теоретический
выход. и ωвых
|
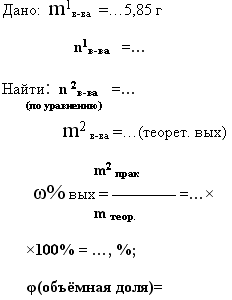
|
-
При действии концентрированной
серной кислоты на кристаллический
хлорид натрия массой 5,85 г было
получено 2 л хлороводорода.
Определите массовую долю выхода
продукта реакции в (%) от теоретически
возможного.
- При взаимодействии цинка с 9,8 г
серной кислоты было получено 14 г
сульфата цинка. Определите массовую
долю выхода продукта реакции в (%) от
теоретически возможного.
- При взаимодействии 23 г натрия с
водой было получено 8,96 л водорода
(н.у.). Найдите объёмную долю выхода
продукта реакции.
- *Песок массой 2 кг сплавили с
избытком гидроксида калия, получив
в результате силикат калия массой 3,82
кг. Определите выход продукта
реакции в % от теоретически
возможного, если массовая доля SiO2
в песке 90%.
|
9. дано: m1в-ва
исход. и ωвых –
найти: m2
в-ва продукта реакции- практический
выход
|
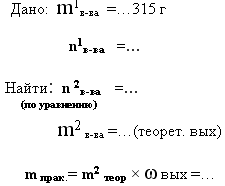
|
-
315 г азотной кислоты полностью
прореагировало с гидроксидом
кальция. Вычислите массу полученного
нитрата кальция, если доля его выхода
составляет 80% от теоретически
возможного.
- Какая масса хлорида железа(III)
будет получена при сжигании 5,6 г
железа в хлоре, если потери его
составляют 10%?
- *Какая масса хлорида железа(III)
будет получена при сжигании 5,6 г
железа в 4,48 л хлора, если потери его
составляют 10%?
- *Цинк массой 6,5 кг обработали 120 кг 10%
раствора серной кислоты. Определите
объём выделившегося газа, если выход
этого продукта реакции составляет 80%
от теоретически возможного.
|
10. дано: m1
в-ва продукта реакции- практический
выход и его ωвых –
найти: m2в-ва
исход.
|
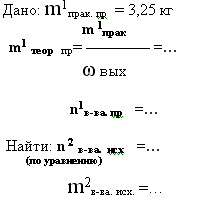
|
-
Сколько граммов сульфида меди(II)
потребуется сжечь, чтобы получить 17,92
л (н.у.) оксида серы (IV),
если выход продукта реакции
составляет 90%?
- Хлорид железа (II)
окислили хлором до хлорида железа(III),
при этом получили 3,25 кг хлорида
железа(III),
что составляет 80% от теоретически
возможного. Какой объём хлора был
израсходован на реакцию.
- *Сколько граммов медной руды,
содержащей 65% сульфида меди(II)
потребуется сжечь, чтобы получить 17,92
л (н.у.) оксида серы (IV),
если выход продукта реакции
составляет 90%?
|
11. дано: m
смеси, m в-ва
(или V в-ва)
прод. реакции, -
найти: mв-ва
и его долю - ω (%)в-ва
в смеси.
А).В реакцию вступает один компонент.
|
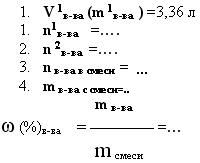
|
-
4,5 г сплава меди с магнием
растворили в соляной кислоте. Объём
выделившегося водорода составил 3,36 л
(н.у.). Какова массовая доля магния в
сплаве.
- 5 г смеси нитрата калия и хлорида
калия растворили в воде и
подействовали раствором нитрата
серебра. Образовался осадок массой 1,5
г. Определите процентный состав
смеси.
- *95,5 г смеси CuO
и Fe2O3
восстановили водородом. На продукт
восстановления подействовали
избытком раствора соляной кислоты.
Объём выделившегося водорода
составил 4,48 л. Каков процентный состав
смеси.
|
- При восстановлении водородом 40 г смеси
меди с оксидом меди(II)
образовалось 6 г воды. Определите массовую
долю (в %) каждого компонента в смеси.
- Определите массовую долю каждого
компонента в смеси, образующейся в
результате взаимодействия 27 г
порошкообразного алюминия и 64 г оксида
железа(III).
- Какая масса 20% соляной кислоты
потребуется для полного растворения 10 г
смеси цинка с оксидом цинка, если при этом
выделился водород объёмом 2,24 л (н.у.).
- Определите массовую долю (в %) железа в
сплаве с углеродом, если при обработке
образца сплава массой 6 г соляной
кислотой выделилось 2,24 л газа (н.у.). Какой
объём соляной кислоты (ρ=
1,09г/мл) с массовой долей HCl
18,25% вступил в реакцию.
- При взаимодействии со щелочью 4,5 г
сплава алюминия с магнием выделилось 3,36 л
водорода (н.у.). Какова массовая доля
алюминия в сплаве?
- Через известковую воду пропустили 1 л
смеси оксида углерода (II)
и оксида углерода(IV).
Выпавший осадок отфильтровали, промыли и
просушили. Его масса составила 2,45 г.
Определите объёмную долю каждого газа в
исходной смеси.
- 4 г смеси кремния, алюминия и оксида
магния обработали избытком соляной
кислоты. Объём выделившегося газа
составил 2,24 л, а масса нерастворившегося
остатка составила 1,2 г. Определите
количество вещества оксида магния в
смеси.
- При растворении 4,5 г оксида меди(II),
загрязнённого песком, был использован 16%-ный
раствор азотной кислоты объёмом 36,1 мл (ρ=
1,093г/мл). Рассчитайте массы чистого оксида
меди и песка, содержащихся в навеске.
В реакцию вступает два компонента. (Составляется
2 уравнения химических реакций и
алгебраическое уравнение или система
уравнений.)
- При взаимодействии смеси порошков
железа и цинка массой 6,05 г с избытком
раствора хлорида меди(II)
образовалась металлическая медь массой 6,4
г. Определите количественный состав
исходной смеси.
- Для растворения смеси карбоната кальция
и карбоната магния в воде потребовалось
2,016 г углекислого газа (н.у.) определите
количественный состав смеси карбонатов.
- При взаимодействии 30,7 г смеси цинка и
алюминия, в разбавленной серной кислоте
выделился водород объёмом 11,2 л (н.у.).
Вычислите массовую долю цинка в смеси.
- На нейтрализацию 100 г раствора,
содержащего 5,7 г смеси гидроксида натрия
и кальция, израсходовали 9,45 г азотной
кислоты. Вычислите массовые доли (в %)
солей в исходной смеси.
- * Смесь железа с оксидом железа(II)
и оксидом железа (III)
обработали соляной кислотой и получили 112
мл водорода. 1 г этой же смеси при
восстановлении водородом даёт 0,2115 г воды.
Определите массовую долю оксида железа в
смеси.