Цели занятия:
Образовательная:
- расширить и углубить знания обучающихся об уровневой организации природы, строении, свойствах и биологической роли неорганических веществ;
- продолжить совершенствование уменийвыделять главную мысль, устанавливать причинно-следственные связи, проводить самоконтроль.
Развивающая: способствовать развитию речи через усложнение и обогащение словарного запаса; умений сравнивать, анализировать, обобщать, формулировать выводы, обосновывать.
Воспитывающая: способствовать формированию научного мировоззрения на основе познаваемости живой природы на микроуровне; сознательного отношения к умственному труду, умения осуществлять самоконтроль хода и результатов учебно-познавательной деятельности, ответственности за результаты труда; привлечению обучающихся к активной познавательной деятельности; воспитаниюсознательной дисциплины и норм поведения, культуры речи.
Тип занятия: урок изучения новых знаний.
Межпредметные связи: Биология человека (9 класс) – состав клетки; биология растений (6 класс) – состав семян; физика – физические свойства воды; химия – первоначальные химические понятия; органические и неорганические вещества, физические и химические свойства воды, диссоциация кислот, растворимые и нерастворимые вещества.
Оборудование: персональные компьютеры, мультимедийный проектор, диаграмма «Распределение элементов в земной коре и в живых организмах», рисунки 8.1.1.1. и 8.1.1.2. мультимедийного курса компании «Физикон» «Открытая биология», видеоролики «Великая тайна воды» (http://www.youtube.com/watch?v=PyvDzXB3m8E&feature=PlayList&p=C0B36056B53178A3&playnext=1&playnext_from=PL&index=17).
Методическая цель: реализация межпредметных связей.
Литература: С.Г.Мамонтов, В.Б.Захаров, Общая биология, М.: Высшая школа, 2000 .
Ход занятия
1. Организационный момент.
2. Актуализация знаний студентов и постановка цели занятия.
Беседа по вопросам и заданиям (работа с оглавлением учебника):
- Какой раздел общей биологии мы изучили? (Раздел 1 «Многообразие живого мира»)
- Изучение какого раздела начнем сегодня? (Раздел 2 «Учение о клетке»)
- Содержание этого раздела распределено в три темы: «Химическая организация клетки», «Строение и функции клетки», «Обмен веществ и энергии клетки». На изучение каждой темы отводится по три занятия
- Какую тему мы начнем изучать сегодня?
Обобщение беседы и постановка цели занятия преподавателем:
Сегодня на занятии мы продолжим изучение клеточного, молекулярного, атомного уровней организации природы, дадим общую характеристику химической организации клетки и более подробно изучим неорганические вещества клетки.
3. Изучение новых знаний.
3.1. Сравнение живой и неживой природы на атомном и молекулярном уровнях организации.
Вступительное слово преподавателя: Клеточный уровень организации природы включает в себя молекулярный уровень, т.е. молекулы химических веществ и атомный уровень, т.е. атомы химических элементов, из которых состоят молекулы химических веществ.
Вопрос: В чем заключается единство живой и неживой природы на атомном уровне организации? (Состоят из атомов одних и тех же элементов.)
Хотя химические элементы живой и неживой природы одинаковы, количественное содержание их атомов различно. Рассмотрим диаграммы (Приложение 1), иллюстрирующие распределение элементов в земной коре и живых организмах.
Задание: Проанализируйте содержание диаграмм и скажите, в чем отличие живой и неживой природы на атомном уровне организации? (В земной коре наиболее распространены атомы кислорода, кремния, алюминия, железа, кальция, натрия, в живых организмах в большем количестве встречаются атомы кислорода, углерода, водорода, азота.)
Химические элементы живой клетки по количественному содержанию атомов делят на группы.
Задание: Составьте схему «Химические элементы клетки», используя текст учебника на страницах 30-31.
Фронтальная проверка выполнения задания.
Задание: Из атомов химических элементов образуются молекулы химических веществ. Подумайте и скажите, в чем принципиальное отличие живой и неживой природы на молекулярном уровне? (B неживой природе могут образовываться молекулы неорганических веществ, а в живой – молекулы неорганических и молекулы органических веществ.)
Задание: Составьте в тетради схему « Химические вещества клетки».
Сегодня на занятии мы более подробно познакомимся с биологической ролью неорганических веществ.
3.2. Строение, свойства и биологическая роль воды.
Демонстрация видеоролика 1 «Великая тайна воды» о распространении и значении воды (Приложение 2).
Задание: Вспомнить из курса химии, записать на доске и объяснить молекулярную, электронную и структурную формулы воды.
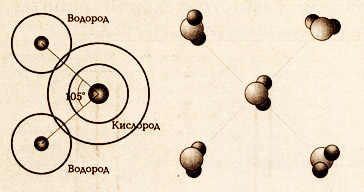
Рис. Схематическое изображение молекул воды
Молекула воды необычна: угол между двумя связями О–Н равен 104°31', а сама молекула имеет большой дипольный момент в результате смещения общей электронной пары к кислороду как более электроотрицательному атому. Так как молекулы воды дипольны, между ними возникают силы электростатического (кулоновского) взаимодействия. Разноименно заряженные атомы разных молекул воды притягиваются и между ними устанавливается нековалентная связь, называемая водородной. При этом каждая молекула воды оказывается довольно прочно связанной с четырьмя соседними молекулами воды, образуются ассоциаты, состоящие как минимум из пяти молекул воды. Теоретически все молекулы воды могут объединиться в одну пространственную сетку, как бы в одну гигантскую макромолекулу, однако водородные связи при движении воды быстро рвутся и также быстро образуются новые. Поэтому между отдельными молекулами воды и ассоциатами существует равновесие.
Большой дипольный момент молекулы воды, водородные связи между молекулами воды обуславливают аномальные свойства воды и ее уникальную биологическую роль.
Задание: Вспомните из курса химии и физики свойства воды и назовите их.
Сообщения обучающихся о свойствах воды (по домашнему заданию, с представлением компьютерной презентации с использованием мультимедийного проектора - по желанию):
Сообщение 1: Образованием ассоциатов объясняются аномальные температуры кипения (100°С), плавления (0°С), высокая теплоемкость воды (удельная теплоемкость воды 4, 184 кДж /(кг* К)) и большая теплота испарения воды. Если бы молекулы воды не объединялись в ассоциаты, то температура кипения согласно положению гидрида кислорода в периодической системе должна быть - 80°С, а температура затвердевания – 100° С., т.е. нормальное состояние воды в условиях Земли было бы газообразным. Плотность при 20° С – 0,9982 г/ см. куб., при 4° С – 1 г/ см. куб., при кристаллизации плотность резко уменьшается - на 9%.
Сообщение 2: Удельная теплоемкость указывает, сколько тепловой энергии необходимо затратить для нагревания 1 кг вещества на один градус. Благодаря высокой теплоемкости воды и ее теплопроводности в клетках равномерно распределяется тепло и происходят минимальные температурные колебания, т. е. поддерживаются постоянные температурные условия для протекания биохимических процессов. При значительном выделении тепловой энергии в клетке, часть ее может использоваться для испарения воды, при этом происходит охлаждение, что также способствует поддержанию постоянных температурных условий внутри клетки.
Сообщение 3: Полярность молекул воды делает ее прекрасным растворителем для других полярных молекул. По отношению к воде молекулы или отдельные части молекул на гидрофильные, т.е. водорастворимые и гидрофобные, т.е. водонерастворимые. Молекулы некоторых веществ содержат как полярные (гидрофильные) так и неполярные (гидрофобные) группы. Такие соединения называются амфифильными. Растворение происходит благодаря гидратации и гидролизу.
Сообщение 4: Еще одно важное свойство воды – большое поверхностное натяжение, которое обусловлено взаимодействием между молекулами воды. Именно поверхностным натяжением объясняются капиллярные явления и передвижение воды по очень тонким каналам , например таким клеткам растений как сосуды и ситовидные трубки.
Сообщение 5: Вода служит не только средой для протекания химических реакций, но и участвует во многих из них.
А) в реакциях фотосинтеза является источником водорода для образования глюкозы.
Б) в реакциях гидролиза высокомолекулярных органических соединений.
Приводятся уравнения соответствующих реакций.
Задание: Соотнесите и запишите в тетрадь свойства воды и биологическую роль воды.
СВОЙСТВА |
БИОЛОГИЧЕСКАЯ РОЛЬ |
Растворитель |
|
Большая теплоемкость |
|
Высокие температуры плавления и кипения |
|
Большая теплота испарения |
|
Поверхностное натяжение |
|
Химический реагент |
|
Биологическая роль воды:
Регулятор теплового баланса клетки (сохранение, распределение и отдача тепла)
Транспорт веществ
Возможность существования жизни
Среда для протекания химических реакций
Образование и расщепление органических веществ.
Демонстрация видеоролика «Великая тайна воды» о свойствах воды (Приложение 3)
3.3. Биологическая роль минеральных солей.
Неорганические вещества находятся в клетках в виде ионов. Основным катионом внутриклеточной среды является К, а внеклеточной – Nа; из анионов – внутри клетки – фосфат-анион, снаружи - хлорид и гидрокарбонат. Для всех живых клеток характерна разница концентраций основных неорганических ионов между внутриклеточным пространством и внеклеточной средой, которые разделены клеточной мембраной. Расчеты показывают, что градиент концентрации ионов по обе стороны мембраны создает в разных клетках потенциал порядка 60-80 мВ (милливольт). Внутренняя сторона клеточной мембраны относительно наружной заряжена отрицательно. Этот градиент существует только у живых клеток, после гибели их он исчезает.
Анионы фосфорной кислоты придают цитоплазме клетки буферные свойства, т. е. Способность поддерживать постоянную слабощелочную реакцию среды.
Задание: Запишите в тетрадь примеры биологической роли катионов, используя текст учебника на стр. 31, 32.
4. Закрепление и коррекция знаний и способов действий студентов.
Задание: Выполните компьютерный тест (cоставлен в программе HyperService).
Сколько химических элементов можно обнаружить в клетке?
а) около 70
б) около 150
в) около 200
Какие химические элементы, содержащиеся в клетке, относят к макроэлементам?
а) S, Na, Са, К
б) О, Н, С, N
в) Ni, Cu, J, Вг.
Функции воды в клетке:
а) передача наследственной информации
б) среда для химических реакций
в) источник энергии.
Неполярные вещества плохо растворяются в воде, так как:
а) их молекулы взаимодействуют с молекулами Н2О сильнее, чем молекулы воды между собой;
б) их молекулы взаимодействуют с молекулами воды слабее, чем молекулы воды между собой;
в) их молекулы взаимодействуют с той же силой, что и молекулы воды между собой.
К гидрофобным веществам относятся
а) соли
б) сахара
в) жиры
В состав гемоглобина входят ионы
а) Mg
б) Fe
в) Zn
Биоэлементами называют химические элементы:
а) входящие в состав живой и неживой природы;
б) входящие в состав неорганических молекул;
в) являющиеся главным компонентом всех органических соединений клетки.
В плазме крови...
а) высокая концентрация ионов Na+ и низкая К+;
б) низкая концентрация ионов Na+ и высокая К+;
в) разницы в концентрации ионов Na+ и К+ нет.
В молекуле воды связь:
а) ионная
б) водородная
в) ковалентная полярная.
На каком уровне организации не наблюдается различие между органическим и неорганическим миром?
а) атомном
б) молекулярном
в) клеточном.
Какие химические элементы, содержащиеся в клетке, относят к микроэлементам?
а) S, Na, Ca, К
б) О, Н, С, N
в) Ni, Cu, J, Вг.
Вода — основа жизни, так как
а) она может находиться в трех состояниях (жидком, твердом и газообразном);
б) является растворителем, обеспечивающим как приток веществ в клетку, так и удаление из нее продуктов обмена;
в) охлаждает поверхность при испарении.
Вещества, хорошо растворимые в воде, называются:
а) гидрофильные
б) гидрофобные
в) амфифильные
Соединения фосфора входят в состав:
а) белков
б) нуклеиновых кислот
в) углеводов.
В состав хлорофилла входят ионы:
а) Fe2+
б) Mg2+
в) Са2+
Соли калия важны для организма, так как:
а) являются катализаторами биохимических реакций;
б) входят в состав гемоглобина;
в) участвуют в проведении нервных импульсов.
Угол между атомами водорода в молекуле воды составляет:
а) 90°
б) 105°
в) 120°
Между молекулами воды связь:
а) ионная
б) водородная
в) ковалентная полярная
5. Подведение итогов занятия.
Анализ степени успешности в овладении содержанием урока и способами деятельности.
Анализ недостатков, ошибок и их причин, поиск путей их преодоления.
6. Консультация по выполнению домашнего задания.
Записи в тетради, по учебнику – стр. 30 – 33.